pH计的基本概念
pH计 是一种分析仪器,用于确定溶液的酸度或碱度——也称为pH。pH 是描述酸度或碱度的度量单位。它以 0 到 14 的等级衡量。
什么是离心?
离心是一种通过施加离心力从溶液中分离颗粒的技术,分离是基于溶液的颗粒大小、形状、密度、粘度和离心转子速度来实现的。
pH 以方程式的形式表示为氢离子浓度的负对数。
例如在纯水或中性溶液中,
pH = -log (1×10-7)
= - (log 1× log10 -7 )
= - (0.0 + (-7.0))
pH = 7.0
pH 计算提供的定量数据以氢离子活性表示酸或碱的活性程度。物质的 pH 值与溶液中氢离子 [H+] 和羟基离子 [OH-] 浓度的比值直接相关。如果 H+ 离子浓度高于 OH-,则材料呈酸性(pH < 7)。如果 OH- 浓度大于 H+ 离子,则材料呈碱性(pH > 7)。如果溶液中存在等量的 H+ 和 OH- 离子,则为中性(pH = 7)。
pH 测量
溶液的 pH 值可以通过 pH 试纸或指示剂来测量,它们会随着 pH 值的变化而改变颜色,但不会给出准确的读数。使用电子 pH 计计算精确的 pH 测量值。pH计由三部分组成:pH测量电极、参比电极和高输入阻抗计。可以将 pH 电极假定为电池,其电压随被测溶液的 pH 值而变化。pH 测量电极是一个对氢离子敏感的玻璃灯泡,其毫伏输出与灯泡内外相对氢离子浓度的变化形成对比。参比电极输出不随氢离子的活度变化。pH 电极具有非常高的内阻,使得电压随 pH 值的变化难以估计。因此,pH 计的输入阻抗和泄漏电阻是至关重要的因素。pH 计是一种高阻抗放大器,可准确测量微小电极电压,并在模拟或数字显示器上以 pH 单位直接显示结果。在某些情况下,也可以读取电压以用于特殊应用或与离子选择性或氧化还原电位 (ORP) 电极一起使用。
pH电极
在过去的 50 到 60 年中,pH 电极技术并没有太大的改革。即使在过去 30 到 40 年的现代技术发展中,pH 电极制造仍然是一门艺术。电极的独特玻璃体由玻璃吹制机吹制成其配置;这不是一项先进或高科技的技术,而是电极制造中非常关键和必不可少的步骤。玻璃的厚度决定了它的电阻并影响它的输出。
一个典型的现代 pH 探头是一个组合电极,它将玻璃电极和参比电极组合成一个整体。复合电极由以下部分组成:
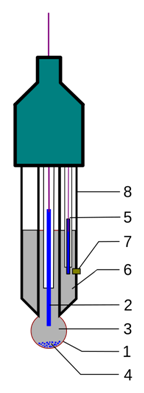
图 2:典型 pH 玻璃电极的示意图。(图片来源维基百科)
电极的感应部分,由特定玻璃制成的灯泡
内电极,通常是氯化银电极或甘汞电极
内部溶液,通常是 pH=7 的缓冲溶液,pH 电极为 0.1 mol/L KCl 或 pM 电极为 0.1 mol/L MCl
使用氯化银电极时,玻璃电极内部会析出少量的AgCl
参比电极,通常与 2 相同
参考内溶液,通常为 0.1 mol/L KCl
与研究溶液的连接,通常由陶瓷或带有石棉或石英纤维的毛细管制成。
电极主体,由非导电玻璃或塑料制成。
pH 电极的底部会膨胀成一个圆形的薄玻璃灯泡。最好将 pH 电极假定为管中的管。内管包含不变的 1×10-7 mol/L HCl 溶液。在内管内部也是参考探头的阴极端。阳极末端包裹在内管外部,并以与内管内部相同类型的参考探针结束。它充满 KCl 参考溶液,并通过用作盐桥的多孔塞与 pH 探头外部的溶液接触。
校准
每次测量前,必须使用至少两种已知 pH 值(通常约为 4 和 7)的标准缓冲溶液校准 pH 计。
一些需要测量 pH 值的典型应用
pH 测量在农业工业中对土壤评估非常重要。主要农作物需要碱性环境,因此必须进行 pH 测量。
它也用于食品工业,特别是用于乳制品,如奶酪、凝乳、酸奶等。
它成为化学和制药行业的强制性要求。
它成为洗涤剂生产中的一个重要因素。
pH 值监测在水处理厂和 RO 净水器中至关重要。
- 上一篇:校准时应该使用哪种pH缓冲溶液?
- 下一篇:pH校准终极指南